Силиконовата в природата (25, 8% в кората)

Характеристики на силиций
физични свойства

Силиконовата - деликатен светлосив материал с метален оттенък или кафяво прахообразно вещество. Структурата на силициев кристал диамант със същия тип, но поради разликите в дължината на връзката между твърдостта на диамантени атоми значително по-висока.
Силиконовата - неметални достъпна за електромагнитно излъчване. Благодарение на някои качество, той е в средата между метали и неметали:
• температурата се повишава до 800 ° С се превръща гъвкави и еластични;
• когато се нагрява до 1417 ° С топи;
• започне да кипи при температура над 2600 ° С;
• промяна на плътността при високо налягане;
• магнитизирана има свойството срещу посоката на външното магнитно поле (диамагнитно).
Силиконовата - полупроводник, и примеса включени в сплавите се определя електрическите характеристики на бъдещите връзки.
химични свойства

Когато нагряването на Si реагира с кислорода, бром, йод, азот, хлор и различни метали. Във връзка с твърди въглеродни сплави са получени с термо - и химиотерапия - резистентност.
Силиконовата няма ефект с водород, така че всички възможни смеси С него получавате по друг начин.
При нормални условия реагира слабо с всички вещества, с изключение на флуор газ. Тъй като се образува силициев тетрафлуорид SiF4. Тази активност е резултат от факта, че повърхността на не-метал поради реакцията с кислород, водна пара и въздух попада филм силициев диоксид и го обгръща. Ето защо, химическата действието се забави леко.
За да се отстрани този слой смес от флуороводородна киселина и азотна киселина или водни алкални разтвори. Някои специална течност за това включва добавяне на хромов анхидрид и други вещества.
силиций е в природата

Силиконовата защото земята е също толкова важно, колкото и въглерод за растения и животни. кора му е почти половината се състои от кислород, и ако прибавим към това и силиция, ще получи 80% от масата. Тази връзка е много важно да се движат на химичните елементи.
75% литосфера съдържа различни соли на силициеви киселини и минерали (пясък, кварцит, кремък, слюди, фелдшпати, и така нататък. D.). По време на образуването на магмата и различни магмени скали Si се натрупва в гранити и ултрабазични скали (плутон и вулканични).
В човешкото тяло, 1 г силикагел. По-голямата част е в костите, сухожилията, кожата и косата, лимфните възли, аортата и трахеята. Той участва в растежа на съединителната и костната тъкан, както и поддържа еластичността на кръвоносните съдове.
Нормалното използване на ден за възрастен - 5-20 мг. Излишният причина силикоза.
Използването на силиций в индустрията
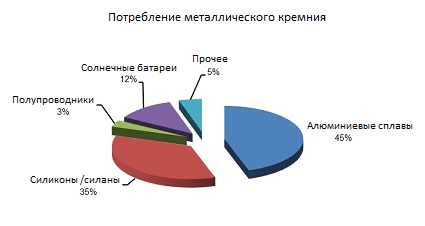
От каменната ера, това неметални известни на човека и е широко използван досега.
• Това е добър редуктор, така че тя се използва в металургията за получаване на метали.
• при определени обстоятелства, силиций е в състояние да провежда електричество, така че тя се използва в областта на електрониката.
• силициевият диоксид се използва в производството на стъкло и силикатни материали.
• специални сплави, използвани за производство на полупроводникови устройства.